剛剛!國(guó)家藥監(jiān)局發(fā)布2019年度藥品審評(píng)報(bào)告
藥通社摘取部分
一����、藥品注冊(cè)申請(qǐng)受理情況
2019年�,藥審中心受理新注冊(cè)申請(qǐng)8082件(含器械組合產(chǎn)品5件��,以受理號(hào)計(jì)����,下同)�����,其中需技術(shù)審評(píng)的注冊(cè)申請(qǐng)6199件(含4907件需藥審中心技術(shù)審評(píng)和行政審批的注冊(cè)申請(qǐng)),直接行政審批(無(wú)需技術(shù)審評(píng)��,下同)的注冊(cè)申請(qǐng)1878件����。
?��。ㄒ唬┛傮w情況
藥審中心受理的8077件藥品注冊(cè)申請(qǐng)中����,化學(xué)藥注冊(cè)申請(qǐng)受理量為6475件���,占2019年全部注冊(cè)申請(qǐng)受理量的80.2%�,2016-2019年各類(lèi)藥品注冊(cè)申請(qǐng)受理情況詳見(jiàn)圖1��。
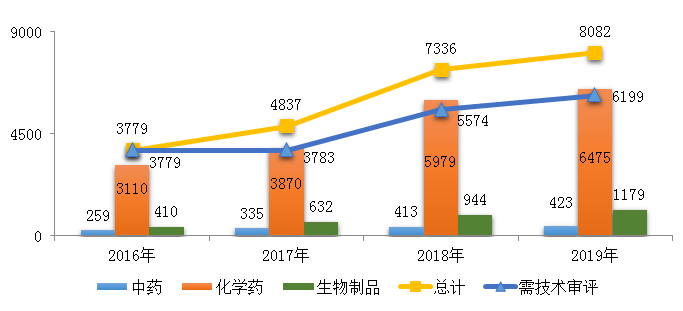
圖1 2016-2019年各類(lèi)藥品注冊(cè)申請(qǐng)受理情況
注:1.2019年受理量中含5件器械組合產(chǎn)品的注冊(cè)申請(qǐng)���,故上圖中2019年受理注冊(cè)申請(qǐng)總量大于中藥����、化學(xué)藥�、生物制品受理注冊(cè)申請(qǐng)之和�;2. 藥審中心的直接行政審批工作自2017年開(kāi)始����,所以2016年無(wú)直接行政審批注冊(cè)申請(qǐng)����,所有受理注冊(cè)申請(qǐng)均需技術(shù)審評(píng)。
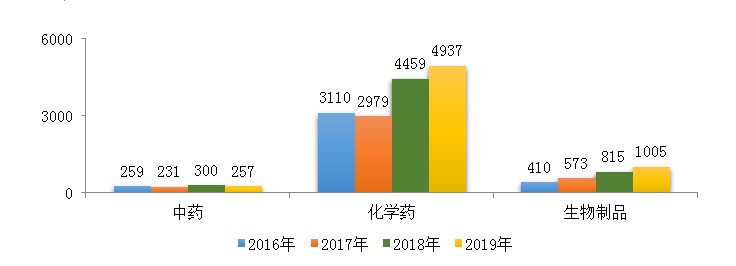
圖2 2017-2019年需技術(shù)審評(píng)的各類(lèi)藥品注冊(cè)申請(qǐng)受理情況
2019年���,受理需技術(shù)審評(píng)的注冊(cè)申請(qǐng)6199件����,較2018年增加11.21%�����,其中化學(xué)藥注冊(cè)申請(qǐng)為4937件�����,較2018年增長(zhǎng)了10.72%,占全部需技術(shù)審評(píng)的注冊(cè)申請(qǐng)受理量的79.64%�;中藥注冊(cè)申請(qǐng)257件�����,較2018年降低了14.33%;生物制品注冊(cè)申請(qǐng)1005件,較2018年增長(zhǎng)了23.3%����。2016-2019年需技術(shù)審評(píng)的化學(xué)藥、中藥和生物制品注冊(cè)申請(qǐng)受理情況詳見(jiàn)圖2�����。
藥審中心受理1類(lèi)創(chuàng)新藥注冊(cè)申請(qǐng)共700件(319個(gè)品種)����,(化學(xué)藥的品種數(shù)以活性成分統(tǒng)計(jì)��,中藥和生物制品的品種數(shù)均以藥品通用名稱(chēng)統(tǒng)計(jì)�����,下同),品種數(shù)較2018年增長(zhǎng)了20.8%�。其中�����,受理1類(lèi)創(chuàng)新藥的新藥臨床試驗(yàn)(IND)申請(qǐng)302個(gè)品種���,較2018年增長(zhǎng)了26.4%�����;受理1類(lèi)創(chuàng)新藥的新藥上市申請(qǐng)(NDA)17個(gè)品種�,較2018年減少了8個(gè)品種���。
?��。ǘ﹪?guó)產(chǎn)創(chuàng)新藥受理情況
藥審中心受理國(guó)產(chǎn)1類(lèi)創(chuàng)新藥注冊(cè)申請(qǐng)528件(244個(gè)品種),其中受理臨床申請(qǐng)503件(228個(gè)品種)���,上市申請(qǐng)25件(16個(gè)品種)����。按藥品類(lèi)型統(tǒng)計(jì)��,化學(xué)藥401件(144個(gè)品種),生物制品127件(100個(gè)品種)�����,創(chuàng)新藥的適應(yīng)癥主要集中在抗腫瘤�����、抗感染和消化系統(tǒng)疾病領(lǐng)域��。
(三)創(chuàng)新藥及原研藥受理情況
藥審中心受理5.1類(lèi)化學(xué)藥原研藥注冊(cè)申請(qǐng)157件(92個(gè)品種)���,受理1類(lèi)創(chuàng)新藥注冊(cè)申請(qǐng)172件(75個(gè)品種),創(chuàng)新藥的適應(yīng)癥主要集中在抗腫瘤�����、內(nèi)分泌和神經(jīng)系統(tǒng)疾病領(lǐng)域。
?���。ㄋ模└黝?lèi)注冊(cè)申請(qǐng)受理情況
1.化學(xué)藥注冊(cè)申請(qǐng)受理情況
藥審中心受理化學(xué)藥注冊(cè)申請(qǐng)6475件�����,其中受理化學(xué)藥IND申請(qǐng)694件�,較2018年增長(zhǎng)了51.9%��;受理化學(xué)藥NDA 130件�,較2018年增長(zhǎng)了21.5%����;受理仿制藥上市申請(qǐng)(ANDA)1047件���,較2018年增長(zhǎng)了6.6%�����;受理一致性評(píng)價(jià)補(bǔ)充申請(qǐng)1038件(308個(gè)品種),件數(shù)較2018年增長(zhǎng)71%�����。2019年化學(xué)藥各類(lèi)注冊(cè)申請(qǐng)受理情況詳見(jiàn)圖3。2016-2019年化學(xué)藥IND申請(qǐng)、NDA和一致性評(píng)價(jià)等注冊(cè)申請(qǐng)受理情況詳見(jiàn)圖4��。
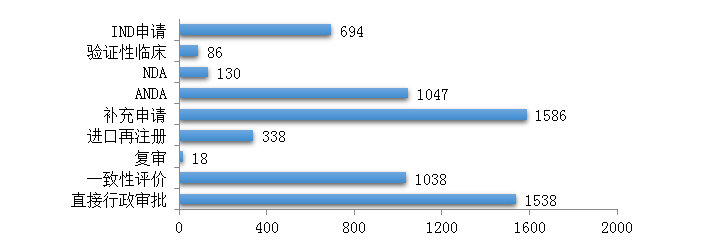
圖3 2019年化學(xué)藥各類(lèi)注冊(cè)申請(qǐng)受理情況
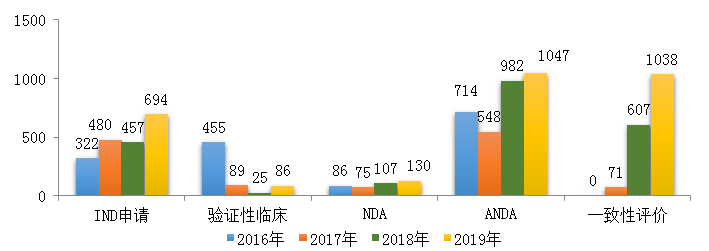
圖4 2016-2019年化學(xué)藥IND申請(qǐng)、NDA和一致性評(píng)價(jià)等注冊(cè)申請(qǐng)受理情況
注:藥審中心自2017年8月開(kāi)始承擔(dān)仿制藥質(zhì)量和療效一致性評(píng)價(jià)工作
?����。?)國(guó)產(chǎn)���、化學(xué)藥IND申請(qǐng)�、NDA受理情況
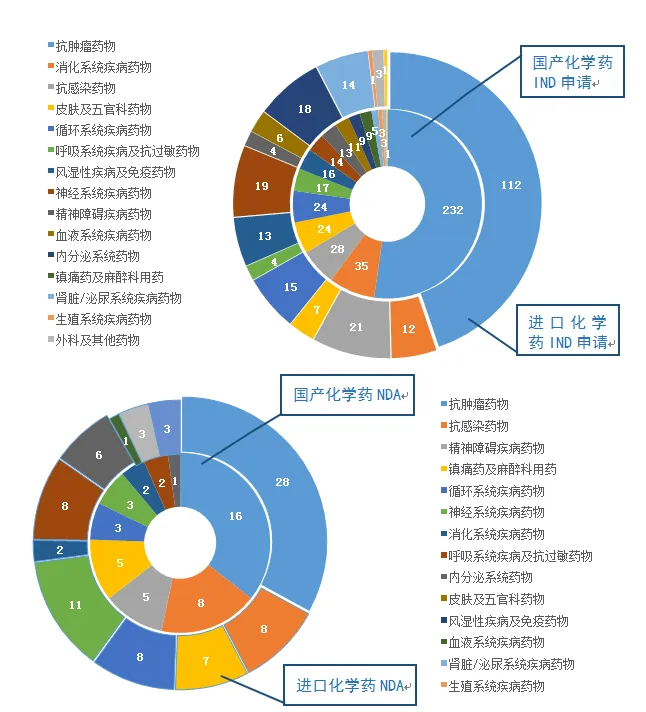
圖5 2019年受理國(guó)產(chǎn)和的化學(xué)藥IND申請(qǐng)��、NDA治療領(lǐng)域分布情況
在化學(xué)藥IND申請(qǐng)中���,受理國(guó)產(chǎn)化學(xué)藥IND申請(qǐng)444件��,受理IND申請(qǐng)250件。國(guó)產(chǎn)化學(xué)藥IND申請(qǐng)的適應(yīng)癥主要集中在抗腫瘤�、消化系統(tǒng)和抗感染藥物領(lǐng)域����,IND申請(qǐng)的適應(yīng)癥主要集中在抗腫瘤���、抗感染藥物和神經(jīng)系統(tǒng)領(lǐng)域。
化學(xué)藥NDA中�����,受理國(guó)產(chǎn)化學(xué)藥NDA 45件,受理化學(xué)藥NDA 85件�����。國(guó)產(chǎn)化學(xué)藥NDA的適應(yīng)癥主要集中在抗腫瘤和抗感染藥物領(lǐng)域�,化學(xué)藥NDA的適應(yīng)癥主要集中在抗腫瘤和神經(jīng)系統(tǒng)領(lǐng)域�����。2019年受理國(guó)產(chǎn)和的化學(xué)藥IND申請(qǐng)�����、NDA治療領(lǐng)域分布情況詳見(jiàn)圖5��。
?。?)1類(lèi)化學(xué)藥創(chuàng)新藥受理情況
藥審中心受理1類(lèi)化學(xué)藥創(chuàng)新藥注冊(cè)申請(qǐng)573件(219個(gè)品種)�,品種數(shù)較2018年增加了39.5%���,其中受理IND申請(qǐng)206個(gè)品種��,較2018年增長(zhǎng)了46.1%��;受理NDA 13個(gè)品種���,較2018年減少了3個(gè)���。
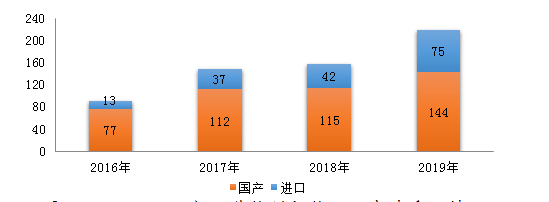
圖6 2016-2019年化學(xué)藥創(chuàng)新藥注冊(cè)申請(qǐng)受理情況
219個(gè)品種的1類(lèi)化學(xué)藥創(chuàng)新藥注冊(cè)申請(qǐng)中,國(guó)產(chǎn)化學(xué)藥創(chuàng)新藥注冊(cè)申請(qǐng)為144個(gè)品種��,化學(xué)藥創(chuàng)新藥注冊(cè)申請(qǐng)為75個(gè)品種。2016-2019年創(chuàng)新藥注冊(cè)申請(qǐng)受理情況詳見(jiàn)圖6��。
2.中藥注冊(cè)申請(qǐng)受理情況
藥審中心受理中藥注冊(cè)申請(qǐng)423件,其中受理中藥IND申請(qǐng)17件�,受理中藥NDA 3件����,受理中藥ANDA 3件�����。2019年中藥各類(lèi)注冊(cè)申請(qǐng)受理情況詳見(jiàn)圖7�。2016-2019年中藥IND申請(qǐng)����、NDA和ANDA受理情況詳見(jiàn)圖8��。
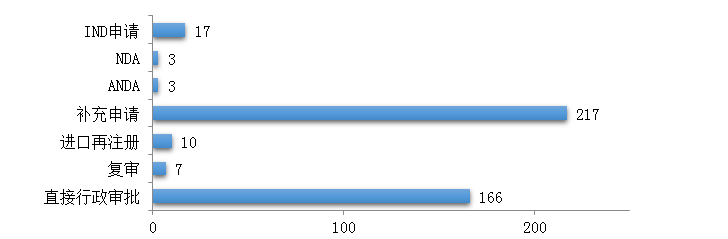
圖7 2019年中藥各類(lèi)注冊(cè)申請(qǐng)受理情況
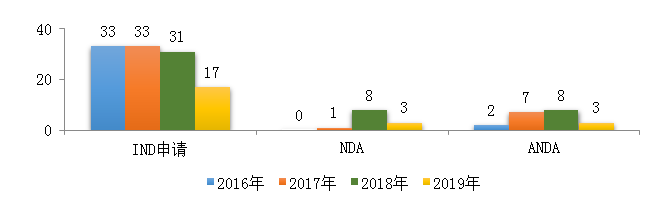
圖8 2016-2019年中藥IND申請(qǐng)����、NDA�����、ANDA受理情況
?��。?)中藥IND申請(qǐng)受理情況
在17件中藥IND申請(qǐng)(5、6�、8類(lèi))中��,適應(yīng)癥主要集中的治療領(lǐng)域?yàn)橄⒑粑凸强?����,占全部中藥IND申請(qǐng)的76%����。
?�。?)中藥新藥受理情況
藥審中心受理5-6類(lèi)中藥新藥注冊(cè)申請(qǐng)18件(18個(gè)品種,無(wú)1-4類(lèi)中藥注冊(cè)申請(qǐng))���,其中中藥IND申請(qǐng)15件(15個(gè)品種),中藥NDA 3件(3個(gè)品種)�,較2018年均有所減少����。
3.生物制品注冊(cè)申請(qǐng)受理情況
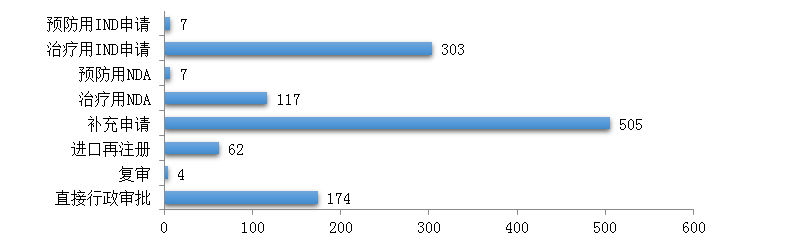
圖9 2019年生物制品各類(lèi)注冊(cè)申請(qǐng)受理情況
藥審中心受理生物制品注冊(cè)申請(qǐng)1179件,其中受理生物制品IND申請(qǐng)310件(預(yù)防用IND申請(qǐng)7件����,治療用IND申請(qǐng)303件),較2018年增長(zhǎng)了4%���;受理生物制品NDA 124件(預(yù)防用NDA 7件,治療用NDA 117件)�����,較2018年增長(zhǎng)了45.9%。2019年生物制品各類(lèi)注冊(cè)申請(qǐng)受理情況詳見(jiàn)圖9�����。2016-2019年生物制品IND申請(qǐng)和NDA受理情況詳見(jiàn)圖10。
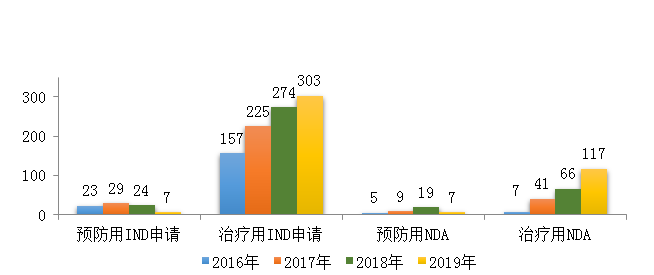
圖10 2016-2019年生物制品IND申請(qǐng)和NDA受理情況
(1)I類(lèi)生物制品創(chuàng)新藥受理情況
藥審中心受理1類(lèi)生物制品創(chuàng)新藥注冊(cè)申請(qǐng)127件(100個(gè)品種)��,件數(shù)較2018年增長(zhǎng)了3.3%,其中預(yù)防用生物制品2件���,治療用生物制品125件�。1類(lèi)生物制品創(chuàng)新藥注冊(cè)申請(qǐng)中���,IND申請(qǐng)121件(96個(gè)品種),較2018年增長(zhǎng)了8%����;NDA 6件(4個(gè)品種���,均為治療用生物制品),較2018年減少了5件���。
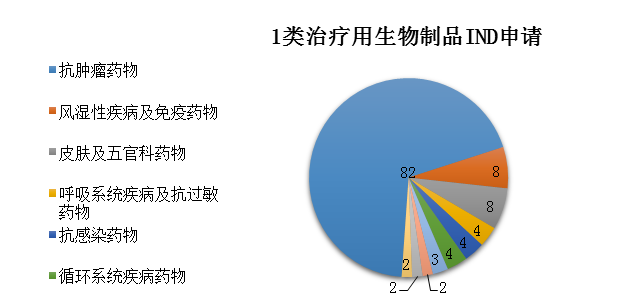
圖11 2019年受理的1類(lèi)治療用生物制品IND申請(qǐng)治療領(lǐng)域分布情況
藥審中心受理1類(lèi)治療用生物制品IND申請(qǐng)119件(95個(gè)品種),適應(yīng)癥主要集中在抗腫瘤治療領(lǐng)域���,占全部1類(lèi)治療用生物制品IND申請(qǐng)的69%��,具體治療領(lǐng)域分布詳見(jiàn)圖11����。
二、藥品注冊(cè)申請(qǐng)審評(píng)審批情況
?��。ㄒ唬┛傮w完成情況
1.全年審評(píng)審批完成情況
2015年至2018年期間藥審中心通過(guò)擴(kuò)充審評(píng)通道��、強(qiáng)化審評(píng)項(xiàng)目管理��、大規(guī)模招聘人員����、借調(diào)省局人員等措施多渠道擴(kuò)增審評(píng)力量、提高審評(píng)效率�����,使得藥品注冊(cè)申請(qǐng)積壓基本得以解決,藥審中心的工作重點(diǎn)已經(jīng)由解決藥品注冊(cè)申請(qǐng)積壓逐漸過(guò)渡為提升藥品注冊(cè)申請(qǐng)的按時(shí)限審評(píng)審批率�,2019年藥審中心實(shí)現(xiàn)了中藥���、化學(xué)藥�����、生物制品各類(lèi)注冊(cè)申請(qǐng)按時(shí)限審評(píng)審批率超過(guò)90%����,基本完成了國(guó)務(wù)院《關(guān)于改革藥品醫(yī)療器械審評(píng)審批制度的意見(jiàn)》(國(guó)發(fā)〔2015〕44號(hào)�����,以下簡(jiǎn)稱(chēng)44號(hào)文件)確定2018年實(shí)現(xiàn)按規(guī)定時(shí)限審批的工作目標(biāo)���。
2019年完成審評(píng)審批的注冊(cè)申請(qǐng)共8730件(含器械組合產(chǎn)品5件)��,其中完成需技術(shù)審評(píng)的注冊(cè)申請(qǐng)6817件(含4075件需藥審中心技術(shù)審評(píng)和行政審批注冊(cè)申請(qǐng))��,完成直接行政審批的注冊(cè)申請(qǐng)1908件��。2019年底在審評(píng)審批和等待審評(píng)審批的注冊(cè)申請(qǐng)已由2015年9月高峰時(shí)的近22000件降至4423件(不含完成審評(píng)因申報(bào)資料缺陷等待申請(qǐng)人回復(fù)補(bǔ)充資料的注冊(cè)申請(qǐng))�,鞏固了44號(hào)文件要求解決注冊(cè)申請(qǐng)積壓的改革成效。
2019年4423件在審評(píng)審批和等待審評(píng)審批的注冊(cè)申請(qǐng)中����,啟動(dòng)審評(píng)3334件�����,審評(píng)結(jié)束等待核查450件�,處于暫停審評(píng)計(jì)時(shí)等待關(guān)聯(lián)品種(290件)、等待申請(qǐng)人核對(duì)質(zhì)標(biāo)說(shuō)明書(shū)包裝標(biāo)簽工藝(235件)�����、等待檢驗(yàn)報(bào)告(36件)等情況中的任務(wù)共639件。
完成技術(shù)審評(píng)的6817件注冊(cè)申請(qǐng)中����,中藥注冊(cè)申請(qǐng)300件����,生物制品注冊(cè)申請(qǐng)1104件,化學(xué)藥注冊(cè)申請(qǐng)為5413件�,化學(xué)藥注冊(cè)申請(qǐng)約占全部審評(píng)完成量的79%��。
2.各類(lèi)注冊(cè)申請(qǐng)審評(píng)完成情況
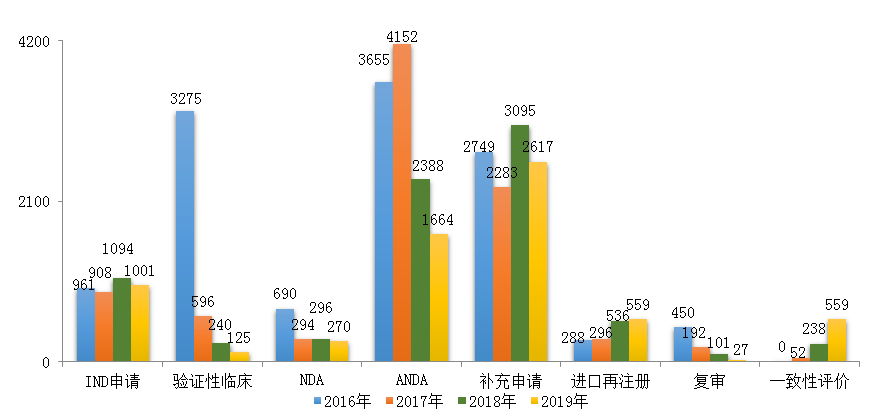
圖12 2016-2019年各類(lèi)注冊(cè)申請(qǐng)審評(píng)完成情況
注:2019年含5件器械組合產(chǎn)品的注冊(cè)申請(qǐng)�����,故上圖中2019年注冊(cè)申請(qǐng)總量大于中藥����、化學(xué)藥��、生物制品注冊(cè)申請(qǐng)之和�����。
藥審中心完成IND申請(qǐng)審評(píng)1001件(含1件器械組合產(chǎn)品)�����,完成NDA審評(píng)270件(含1件器械組合產(chǎn)品)�,完成ANDA審評(píng)1664件(含3件藥械組合產(chǎn)品)����。2016-2019年各類(lèi)注冊(cè)申請(qǐng)審評(píng)完成情況詳見(jiàn)圖12��。
3.審評(píng)通過(guò)情況
2019年�,藥審中心審評(píng)通過(guò)批準(zhǔn)IND申請(qǐng)926件���,審評(píng)通過(guò)NDA 164件��,審評(píng)通過(guò)ANDA 654件,審評(píng)通過(guò)批準(zhǔn)口服固體制劑一致性評(píng)價(jià)申請(qǐng)260件(按活性成分統(tǒng)計(jì)95個(gè)品種���,按通用名統(tǒng)計(jì)107個(gè)品種���,詳見(jiàn)附表1),品種數(shù)較2018年(57個(gè)品種)同比增長(zhǎng)66.7%�����。
審評(píng)通過(guò)上市1類(lèi)創(chuàng)新藥10個(gè)品種,審評(píng)通過(guò)原研藥58個(gè)品種(含新適應(yīng)癥)����,具體品種詳見(jiàn)附表2�、3���。
(二)化學(xué)藥注冊(cè)申請(qǐng)審評(píng)完成情況
1.總體情況
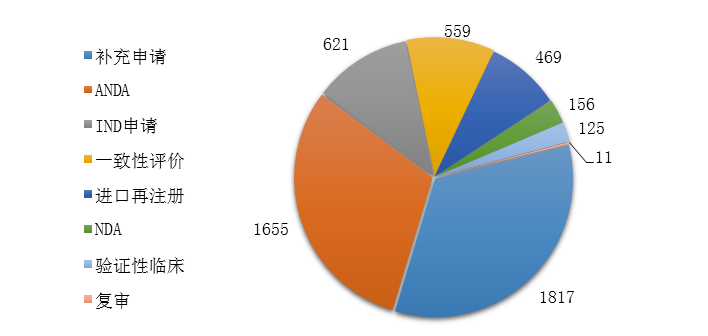
圖13 2019年化學(xué)藥各類(lèi)注申請(qǐng)的審評(píng)完成情況
藥審中心完成審評(píng)的化學(xué)藥注冊(cè)申請(qǐng)5413件��,其中完成化學(xué)藥臨床申請(qǐng)(IND申請(qǐng)和驗(yàn)證性臨床)共746件��,完成化學(xué)藥NDA 156件�,完成化學(xué)藥ANDA 1655件�����。2019年化學(xué)藥各類(lèi)注冊(cè)申請(qǐng)的審評(píng)完成情況詳見(jiàn)圖13。
2.審評(píng)通過(guò)情況
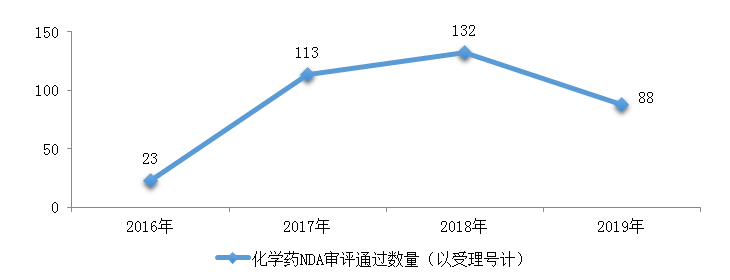 圖14 2016-2019年化學(xué)藥NDA審評(píng)通過(guò)數(shù)量情況
圖14 2016-2019年化學(xué)藥NDA審評(píng)通過(guò)數(shù)量情況
表1 2019年化學(xué)藥各類(lèi)注冊(cè)申請(qǐng)審評(píng)完成的具體情況
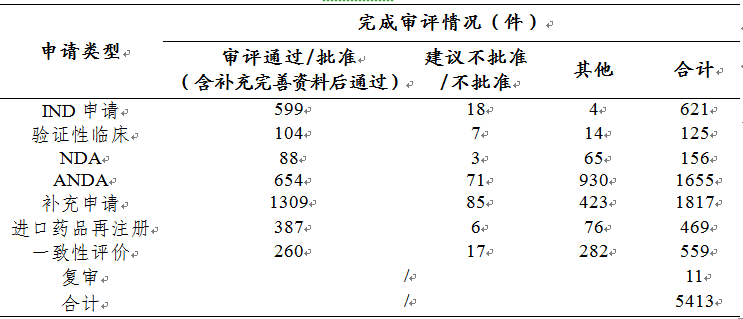 注:“其他”是指申請(qǐng)人主動(dòng)申請(qǐng)撤回的注冊(cè)申請(qǐng)����、完成審評(píng)等待申請(qǐng)人補(bǔ)充完善申報(bào)資料的注冊(cè)申請(qǐng)、非藥審中心審評(píng)報(bào)送國(guó)家局藥品注冊(cè)管理司的注冊(cè)申請(qǐng)����、送國(guó)家局醫(yī)療器械技術(shù)審評(píng)中心的藥械組合注冊(cè)申請(qǐng)和關(guān)聯(lián)制劑撤回的原料/輔料注冊(cè)申請(qǐng)等�,下同���。
注:“其他”是指申請(qǐng)人主動(dòng)申請(qǐng)撤回的注冊(cè)申請(qǐng)����、完成審評(píng)等待申請(qǐng)人補(bǔ)充完善申報(bào)資料的注冊(cè)申請(qǐng)、非藥審中心審評(píng)報(bào)送國(guó)家局藥品注冊(cè)管理司的注冊(cè)申請(qǐng)����、送國(guó)家局醫(yī)療器械技術(shù)審評(píng)中心的藥械組合注冊(cè)申請(qǐng)和關(guān)聯(lián)制劑撤回的原料/輔料注冊(cè)申請(qǐng)等�,下同���。
藥審中心完成審評(píng)的化學(xué)藥NDA共156件��,其中審評(píng)通過(guò)88件。2016-2019年化學(xué)藥NDA審評(píng)通過(guò)數(shù)量情況詳見(jiàn)圖14�,2019年化學(xué)藥各類(lèi)注冊(cè)申請(qǐng)審評(píng)完成的具體情況詳見(jiàn)表1����。
藥審中心完成審評(píng)的化學(xué)藥IND申請(qǐng)621件,審評(píng)通過(guò)批準(zhǔn)IND申請(qǐng)599件�,其中批準(zhǔn)1類(lèi)化學(xué)藥創(chuàng)新藥IND申請(qǐng)493件(189個(gè)品種)�����。2016-2019年1類(lèi)化學(xué)藥創(chuàng)新藥IND申請(qǐng)審評(píng)通過(guò)批準(zhǔn)數(shù)量詳見(jiàn)圖15�。
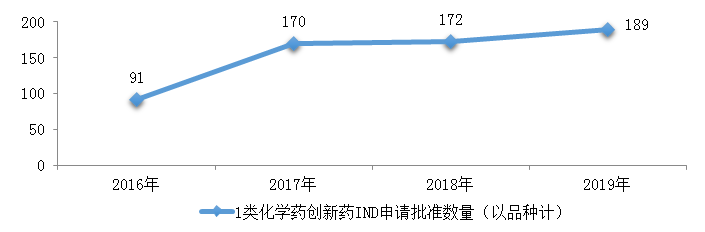
圖15 2016-2019年1類(lèi)化學(xué)藥創(chuàng)新藥IND申請(qǐng)批準(zhǔn)數(shù)量
藥審中心批準(zhǔn)IND申請(qǐng)的189個(gè)1類(lèi)化學(xué)藥創(chuàng)新藥中���,抗腫瘤藥物���、消化系統(tǒng)疾病藥物���、抗感染藥物和神經(jīng)系統(tǒng)疾病藥物較多,占全部創(chuàng)新藥臨床試驗(yàn)批準(zhǔn)數(shù)量的70%����。2019年審評(píng)審批IND申請(qǐng)的1類(lèi)化學(xué)藥創(chuàng)新藥適應(yīng)癥分布詳見(jiàn)圖16��。
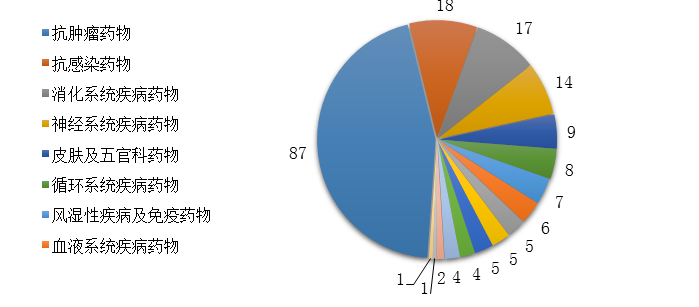 圖16 2019年審評(píng)審批IND申請(qǐng)的1類(lèi)化學(xué)藥創(chuàng)新藥適應(yīng)癥分布
圖16 2019年審評(píng)審批IND申請(qǐng)的1類(lèi)化學(xué)藥創(chuàng)新藥適應(yīng)癥分布
注:部分化學(xué)藥創(chuàng)新藥有多個(gè)適應(yīng)癥分布在不同的適應(yīng)癥分組中�����,故上圖中各適應(yīng)癥分組創(chuàng)新藥品種數(shù)之和大于189個(gè)���。
?��。ㄈ┲兴幾?cè)申請(qǐng)審評(píng)完成情況
1.總體情況
藥審中心完成審評(píng)的中藥注冊(cè)申請(qǐng)300件���,其中完成IND申請(qǐng)17件�,完成NDA 3件�����,完成ANDA 6件���。2019年中藥各類(lèi)注冊(cè)申請(qǐng)的審評(píng)完成情況詳見(jiàn)圖17。
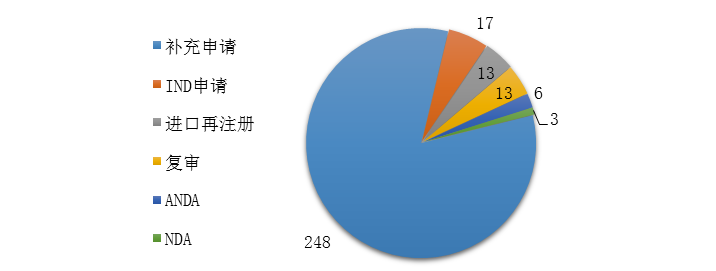
圖17 2019年中藥各類(lèi)注冊(cè)申請(qǐng)的審評(píng)完成情況
2.審評(píng)通過(guò)情況
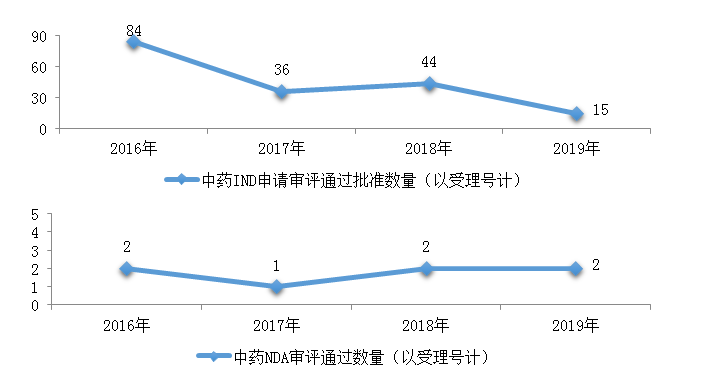
圖18 2016-2019年中藥IND申請(qǐng)審評(píng)通過(guò)批準(zhǔn)和NDA審評(píng)通過(guò)數(shù)量
藥審中心審評(píng)通過(guò)批準(zhǔn)中藥IND申請(qǐng)15件����,審評(píng)通過(guò)中藥NDA 2件(2個(gè)品種���,芍麻止痙顆粒、小兒荊杏止咳顆粒)�����。2019年中藥各類(lèi)注冊(cè)申請(qǐng)審評(píng)完成的具體情況詳見(jiàn)表2�,2016-2019年中藥IND申請(qǐng)審評(píng)通過(guò)批準(zhǔn)和NDA審評(píng)通過(guò)數(shù)量詳見(jiàn)圖18�����。
表2 2019年中藥各類(lèi)注冊(cè)申請(qǐng)審評(píng)完成的具體情況

藥審中心審評(píng)通過(guò)批準(zhǔn)的中藥IND申請(qǐng)15件���,涉及10個(gè)適應(yīng)癥領(lǐng)域�����,其中心血管�、消化、腫瘤�����、呼吸、腎臟各2件����,共占67%���,具體治療領(lǐng)域分布詳見(jiàn)圖19。
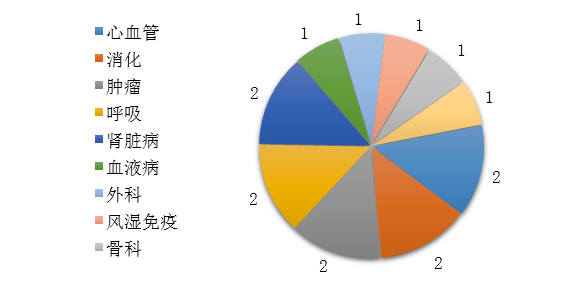
圖19 2019年批準(zhǔn)IND申請(qǐng)的中藥適應(yīng)癥分布
?��。ㄋ模┥镏破纷?cè)申請(qǐng)審評(píng)完成情況
1.總體情況
藥審中心完成審評(píng)的生物制品注冊(cè)申請(qǐng)共1104件���,其中完成預(yù)防用生物制品IND申請(qǐng)(預(yù)防用IND申請(qǐng))24件����,完成治療用生物制品IND申請(qǐng)(治療用IND申請(qǐng))338件����,完成預(yù)防用生物制品NDA(預(yù)防用NDA)13件���,完成治療用生物制品NDA(治療用NDA)95件����,完成體外診斷試劑NDA(體外診斷NDA)2件。2019年生物制品各類(lèi)注冊(cè)申請(qǐng)的審評(píng)完成情況詳見(jiàn)圖20�。
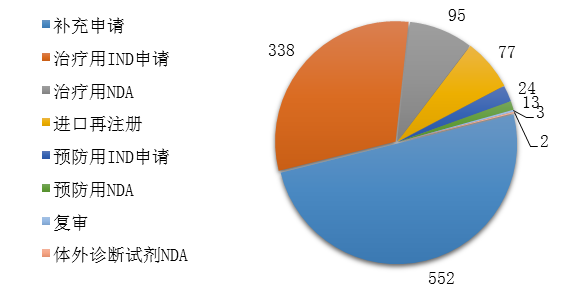
圖20 2019年生物制品各類(lèi)注冊(cè)申請(qǐng)的審評(píng)完成情況
2.審評(píng)通過(guò)情況
藥審中心審評(píng)通過(guò)批準(zhǔn)預(yù)防用IND申請(qǐng)18件����、治療用IND申請(qǐng)294件,審評(píng)通過(guò)預(yù)防用NDA 5件����、治療用NDA 67件、體外診斷NDA 2件���。2019年生物制品各類(lèi)注冊(cè)申請(qǐng)審評(píng)完成的具體情況詳見(jiàn)表3����,2016-2019生物制品IND申請(qǐng)審評(píng)通過(guò)批準(zhǔn)和NDA審評(píng)通過(guò)數(shù)量詳見(jiàn)圖21����。
表3 2019年生物制品各類(lèi)注冊(cè)申請(qǐng)審評(píng)完成的具體情況
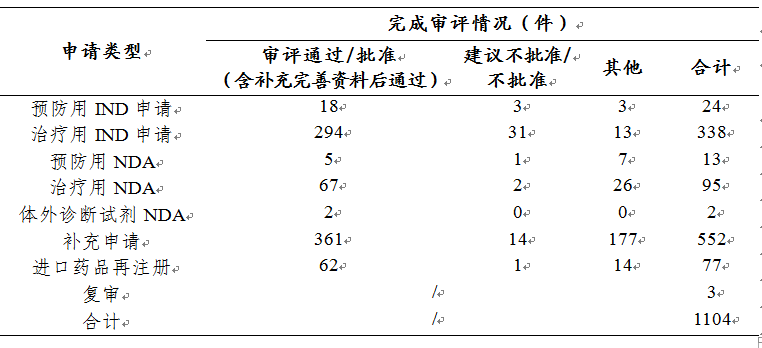
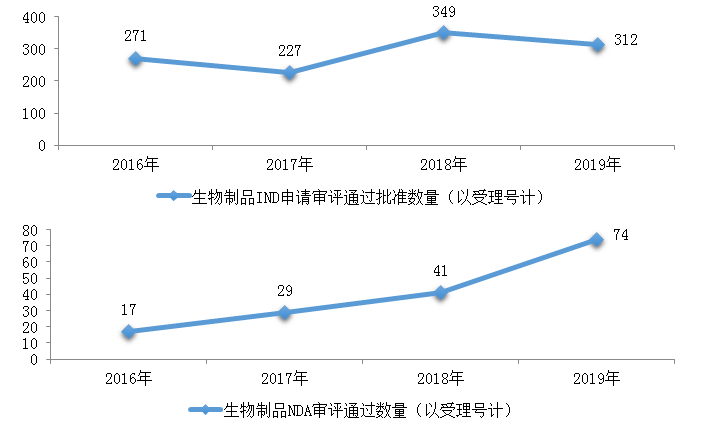
圖21 2016-2019年生物制品IND申請(qǐng)審評(píng)通過(guò)批準(zhǔn)和NDA審評(píng)通過(guò)數(shù)量
藥審中心審評(píng)通過(guò)批準(zhǔn)生物制品IND申請(qǐng)312件,治療領(lǐng)域分布詳見(jiàn)圖22�����。
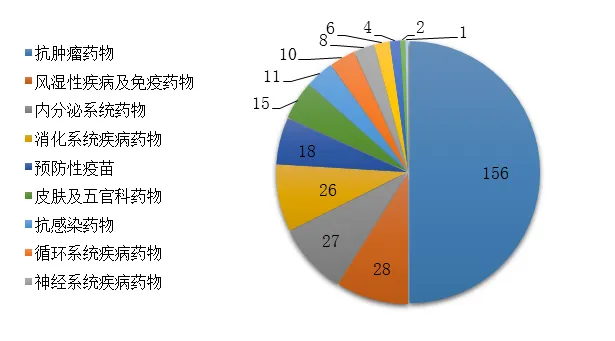
圖22 2019年批準(zhǔn)的生物制品IND申請(qǐng)適應(yīng)癥分布
藥審中心審評(píng)通過(guò)批準(zhǔn)生物制品NDA 74件,治療領(lǐng)域分布詳見(jiàn)圖23�。
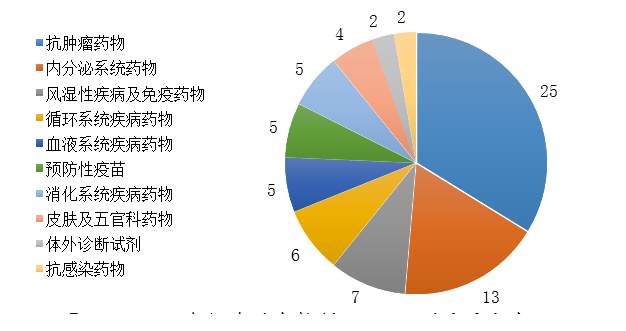
圖23 2019年批準(zhǔn)的生物制品NDA適應(yīng)癥分布
?���。ㄎ澹┬姓徟?cè)申請(qǐng)完成情況
1.總體情況
2019年���,藥審中心完成行政審批中藥��、化學(xué)藥、生物制品注冊(cè)申請(qǐng)5983件�,其中完成審評(píng)審批的注冊(cè)申請(qǐng)(臨床試驗(yàn)申請(qǐng)���、一致性評(píng)價(jià)、補(bǔ)充申請(qǐng)���、藥品再注冊(cè)申請(qǐng)及復(fù)審)4075件����,完成直接行政審批的注冊(cè)申請(qǐng)(無(wú)需技術(shù)審評(píng)的補(bǔ)充申請(qǐng)、臨時(shí)申請(qǐng))1908件���。
2.審評(píng)審批完成情況
4075件需藥審中心審評(píng)審批的注冊(cè)申請(qǐng)中,臨床試驗(yàn)申請(qǐng)1124件(含驗(yàn)證性臨床)�、一致性評(píng)價(jià)345件�、補(bǔ)充申請(qǐng)2127件����、藥品再注冊(cè)申請(qǐng)471件��、復(fù)審8件。按照臨床試驗(yàn)60日默示許可制度�,藥審中心完成審評(píng)審批后發(fā)出臨床試驗(yàn)通知書(shū)1178份�,含1066份《臨床試驗(yàn)通知書(shū)》和112份《暫停臨床試驗(yàn)通知書(shū)》。因ANDA等注冊(cè)申請(qǐng)?jiān)诩夹g(shù)審評(píng)過(guò)程中需申請(qǐng)人補(bǔ)充臨床試驗(yàn)����,藥審中心會(huì)以《臨床試驗(yàn)通知書(shū)》的形式告知申請(qǐng)人,故臨床試驗(yàn)通知書(shū)發(fā)出數(shù)量大于需藥審中心審評(píng)審批的臨床試驗(yàn)申請(qǐng)1124件�。
3.直接行政審批完成情況
1908件藥審中心技術(shù)審評(píng)的直接行政審批注冊(cè)申請(qǐng)中��,補(bǔ)充申請(qǐng)1491件��、臨時(shí)申請(qǐng)417件。
1908件藥審中心直接行政審批注冊(cè)申請(qǐng)平均審批時(shí)限為9.9個(gè)工作日�����,其中有1905件在法定的20日時(shí)限內(nèi)完成,全年平均按時(shí)限完成率為99.8%��。
(六)優(yōu)先審評(píng)情況
1.優(yōu)先審評(píng)品種納入情況
根據(jù)原國(guó)家食品藥品監(jiān)督管理總局(以下簡(jiǎn)稱(chēng)原總局)《關(guān)于解決藥品注冊(cè)申請(qǐng)積壓實(shí)行優(yōu)先審評(píng)審批的意見(jiàn)》(食藥監(jiān)藥化管〔2016〕19號(hào))和《關(guān)于鼓勵(lì)藥品創(chuàng)新實(shí)行優(yōu)先審評(píng)審批的意見(jiàn)》(食藥監(jiān)藥化管〔2017〕126號(hào))����,2019年藥審中心將253件(按通用名計(jì)139個(gè)品種)注冊(cè)申請(qǐng)納入優(yōu)先審評(píng)程序�,同比降低19.2%��,其中兒童用藥和罕見(jiàn)病用藥52件���。2016-2019年納入優(yōu)先審評(píng)程序的各類(lèi)注冊(cè)申請(qǐng)情況詳見(jiàn)表4。
表4 2016-2019年納入優(yōu)先審評(píng)程序的注冊(cè)申請(qǐng)情況
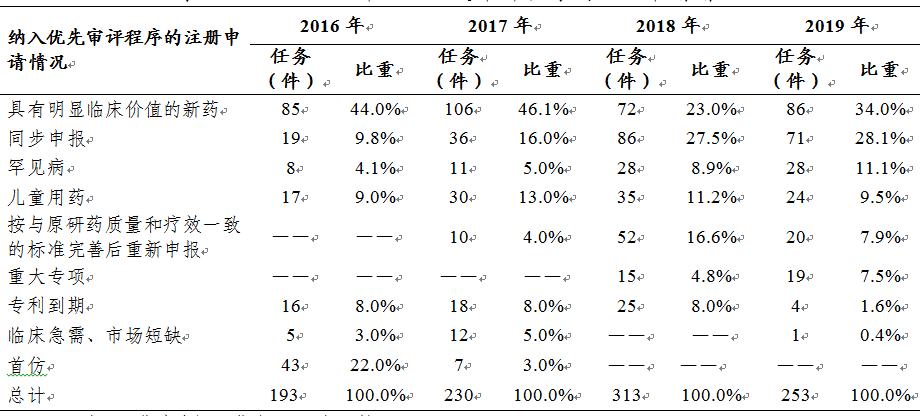
注:1.優(yōu)先審評(píng)工作自2016年開(kāi)始�。
2. 比重=當(dāng)年各類(lèi)任務(wù)/任務(wù)總量���,下同�。
在已納入優(yōu)先審評(píng)的注冊(cè)申請(qǐng)中�����,具有明顯臨床價(jià)值的新藥占比34%���,所占比例最大����,其次為同步申報(bào)品種(28.1%)。與2018年已納入優(yōu)先審評(píng)注冊(cè)申請(qǐng)的結(jié)構(gòu)相比較���,具有明顯臨床價(jià)值的新藥占比由23%增至34%����,按與原研藥質(zhì)量和療效一致的標(biāo)準(zhǔn)完善后重新申報(bào)品種占比則由16.6%降至7.9%�����,從數(shù)據(jù)變化上來(lái)看��,仿制藥數(shù)量逐漸減少�,優(yōu)先審評(píng)資源更多的聚焦到具有明顯臨床價(jià)值、臨床急需和臨床優(yōu)勢(shì)的藥品上來(lái)�����。
2.優(yōu)先審評(píng)品種完成情況
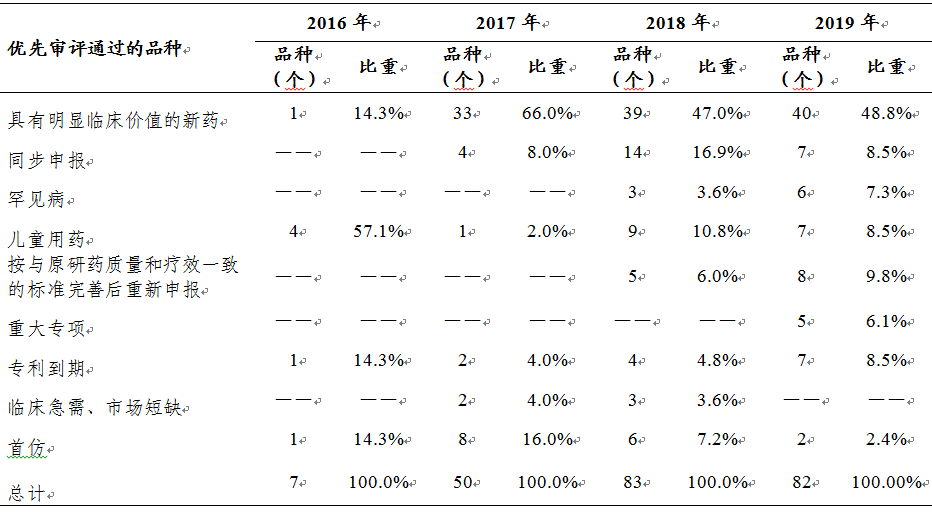
2019年有143件注冊(cè)申請(qǐng)(按通用名計(jì)82個(gè)品種)通過(guò)優(yōu)先審評(píng)程序���,得以加快批準(zhǔn)上市���,如我國(guó)自主研發(fā)的1類(lèi)創(chuàng)新藥注射用甲苯磺酸瑞馬唑侖�、甘露特鈉膠囊����,治療罕見(jiàn)病法布雷病注射用阿加糖酶β,新型核因子κB受體激活因子配體(RANKL)抑制劑地舒單抗注射液����,治療糖尿病的聚乙二醇洛塞那肽注射液�、治療銀屑病的本維莫德乳膏�����、非小細(xì)胞肺癌靶向治療藥物達(dá)可替尼片等藥品��。近幾年優(yōu)先審評(píng)的品種情況詳見(jiàn)表5����,具體品種名單詳見(jiàn)附表4���。
表5 2016-2019年優(yōu)先審評(píng)通過(guò)的品種情況
?��。ㄆ撸贤ń涣髑闆r
1.總體情況
為進(jìn)一步強(qiáng)化服務(wù)意識(shí)��,為申請(qǐng)人研發(fā)創(chuàng)新提供便捷的指導(dǎo)和服務(wù)��,藥審中心不斷豐富溝通交流渠道�,提高溝通交流效率和質(zhì)量�����,形成了溝通交流會(huì)議���、一般性技術(shù)問(wèn)題咨詢(xún)���、電話咨詢(xún)、郵件咨詢(xún)和現(xiàn)場(chǎng)咨詢(xún)的多渠道���、多層次的溝通交流模式�����。
2019年藥審中心接收溝通交流會(huì)議申請(qǐng)2633件�,較2018年增長(zhǎng)了32.8%��,辦理溝通交流會(huì)議申請(qǐng)1871件���,較2018年增長(zhǎng)了41.1%����。藥審中心為保證會(huì)議質(zhì)量��、提高會(huì)議效率,按照國(guó)家局《關(guān)于發(fā)布藥品研發(fā)與技術(shù)審評(píng)溝通交流管理辦法的公告》(2018年第74號(hào))相關(guān)要求,在會(huì)前嚴(yán)格篩選�,剔除了存在重復(fù)提交和未提供有效會(huì)議資料等問(wèn)題的會(huì)議申請(qǐng)��,經(jīng)過(guò)審核的會(huì)議申請(qǐng)����,按時(shí)限要求盡快召開(kāi)溝通交流會(huì)議����。對(duì)于無(wú)需召開(kāi)會(huì)議的申請(qǐng),藥審中心均采用書(shū)面回復(fù)的形式及時(shí)反饋申請(qǐng)人。
2019年在網(wǎng)絡(luò)平臺(tái)接收一般性技術(shù)問(wèn)題咨詢(xún)16572個(gè)�����,較2018年增長(zhǎng)了8.9%;接收電話咨詢(xún)超過(guò)上萬(wàn)次���,郵件咨詢(xún)數(shù)千件�,同時(shí)也面向社會(huì)提供現(xiàn)場(chǎng)咨詢(xún)服務(wù)�。近幾年接收溝通交流申請(qǐng)和一般性技術(shù)問(wèn)題咨詢(xún)具體情況詳見(jiàn)圖24��。
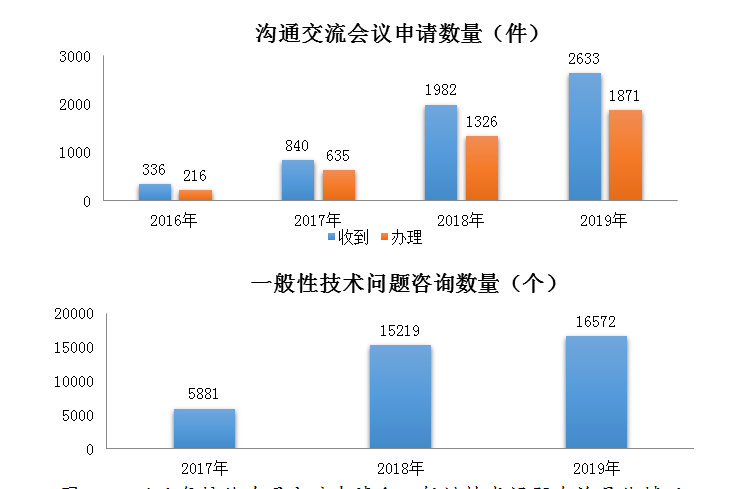
圖24 近幾年接收溝通交流申請(qǐng)和一般性技術(shù)問(wèn)題咨詢(xún)具體情況
注:一般性技術(shù)問(wèn)題的解答工作自2017年開(kāi)始。
2.溝通交流會(huì)議申請(qǐng)的完成情況
表6 2019年各類(lèi)溝通交流會(huì)議申請(qǐng)及辦理情況
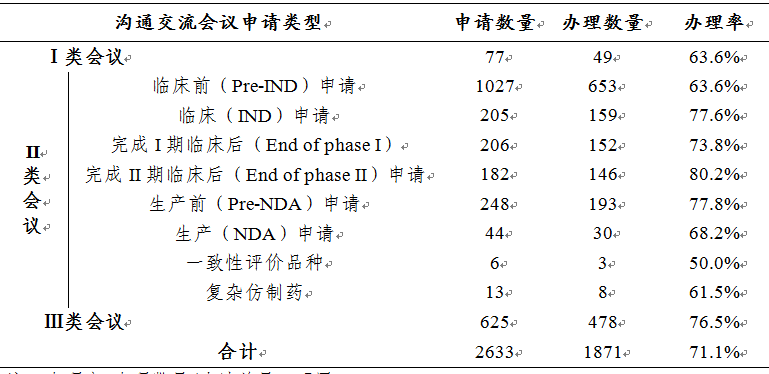
注:辦理率=辦理數(shù)量/申請(qǐng)總量����,下同����。
在藥審中心所辦理的1871件溝通交流會(huì)議申請(qǐng)中,在藥物研發(fā)關(guān)鍵階段召開(kāi)的II類(lèi)會(huì)議所占比例較大�,為71.8%,而II類(lèi)會(huì)議中Pre-IND會(huì)議申請(qǐng)占比最多��,為34.9%�。2019年各類(lèi)溝通交流會(huì)議申請(qǐng)及辦理情況詳見(jiàn)表6�����。
表7 2018-2019年各類(lèi)溝通交流會(huì)議召開(kāi)情況
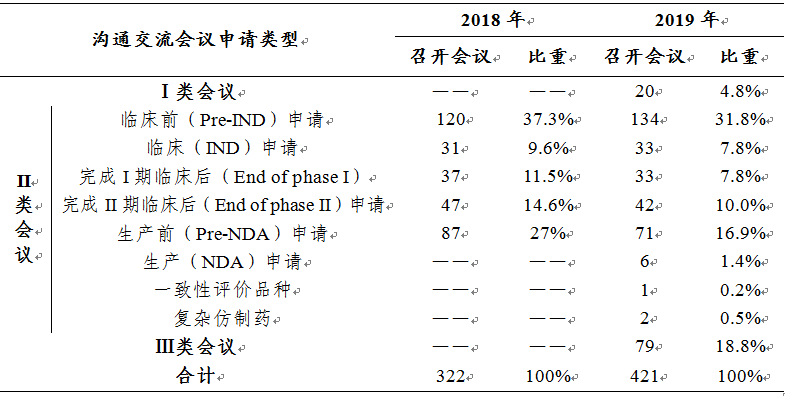
溝通交流會(huì)議的形式為電話會(huì)議��、視頻會(huì)議�����、面對(duì)面會(huì)議�。2019年召開(kāi)了溝通交流會(huì)議421次����,較2018年(322次)增長(zhǎng)30.7%�����。2018-2019年各類(lèi)溝通交流會(huì)議的召開(kāi)情況詳見(jiàn)表7。
3.一般性技術(shù)問(wèn)題答復(fù)情況
在藥審中心網(wǎng)站上接收了社會(huì)公眾16572個(gè)一般性技術(shù)問(wèn)題的咨詢(xún)。總體上,按照內(nèi)容分類(lèi),公眾咨詢(xún)的問(wèn)題主要集中于原輔包(4152個(gè))����、受理(1846個(gè))等方面�����;按照藥品分類(lèi)����,公眾咨詢(xún)的問(wèn)題主要集中于化學(xué)藥物(9743個(gè)),并且集中于化學(xué)藥一致性評(píng)價(jià)(1386個(gè))�����、化學(xué)藥受理(1174個(gè))等方面。一般性技術(shù)問(wèn)題答復(fù)具體情況詳見(jiàn)表8�。
表8 一般性技術(shù)問(wèn)題答復(fù)具體情況
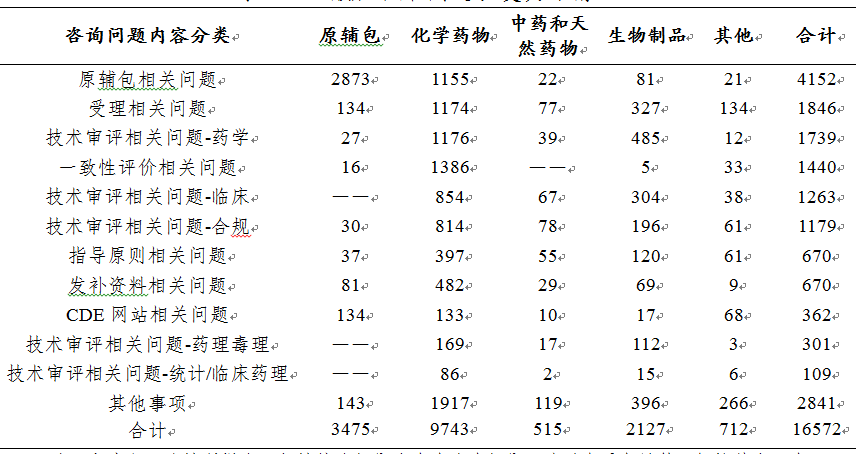
注:申請(qǐng)人一次性所提出一般性技術(shù)問(wèn)題中含有多個(gè)問(wèn)題��,為避免重復(fù)計(jì)算����,僅按其中一個(gè)問(wèn)題的類(lèi)型進(jìn)行統(tǒng)計(jì)�。
(八)核查檢查情況
2019年��,藥審中心基于技術(shù)審評(píng)需要和申請(qǐng)人合規(guī)情況���,啟動(dòng)核查任務(wù)1230個(gè),其中藥學(xué)現(xiàn)場(chǎng)核查任務(wù)782個(gè)�����,臨床試驗(yàn)數(shù)據(jù)核查任務(wù)446個(gè)���,藥理毒理研究核查任務(wù)2個(gè)。
2019年,藥審中心接收核查報(bào)告1242份,其中藥學(xué)現(xiàn)場(chǎng)檢查報(bào)告689份���,臨床試驗(yàn)核查報(bào)告551份�����,藥理毒理研究核查報(bào)告2個(gè)�。
此外��,基于投訴舉報(bào)和審評(píng)發(fā)現(xiàn)的問(wèn)題�����,2019年藥審中心啟動(dòng)有因檢查12個(gè)��,接收有因檢查報(bào)告8份。
三�����、重點(diǎn)治療領(lǐng)域品種
抗腫瘤藥物:
1.甲磺酸氟馬替尼片��,為我國(guó)首個(gè)具有自主知識(shí)產(chǎn)權(quán)的小分子Bcr-abl酪氨酸激酶抑制劑��,適用于治療費(fèi)城染色體陽(yáng)性的慢性髓性白血病慢性期成人患者��,本品獲批上市為此類(lèi)患者提供了更好的治療選擇�。
2.達(dá)可替尼片,為第二代小分子表皮生長(zhǎng)因子受體(EGFR)酪氨酸激酶抑制劑(TKI)����,適用于局部晚期或轉(zhuǎn)移性表皮生長(zhǎng)因子受體敏感突變的非小細(xì)胞肺癌患者的一線治療。與第一代EGFR-TKI相比���,本品可延長(zhǎng)患者的生存期�����,為此類(lèi)患者提供了更好的治療手段��。
3.甲苯磺酸尼拉帕利膠囊���,為一種高選擇性的多聚腺苷5'二磷酸核糖聚合酶(PARP)抑制劑創(chuàng)新藥物���,適用于鉑敏感的復(fù)發(fā)性上皮性卵巢癌、輸卵管癌或原發(fā)性腹膜癌成人患者在含鉑化療達(dá)到完全緩解或部分緩解后的維持治療�����,本品獲批上市為此類(lèi)患者提供了新的治療選擇。
4.地舒單抗注射液�,為核因子κB受體激活因子配體(RANKL)的全人化單克隆IgG2抗體,適用于治療不可手術(shù)切除或者手術(shù)切除可能導(dǎo)致嚴(yán)重功能障礙的骨巨細(xì)胞瘤��,屬臨床急需境外新藥名單品種��。本品獲批上市填補(bǔ)了此類(lèi)患者的治療空白����,滿(mǎn)足其迫切的臨床需求。
5.達(dá)雷妥尤單抗注射液����,為全球首個(gè)抗CD38單克隆抗體,也是用于治療多發(fā)性骨髓瘤的首個(gè)單克隆抗體���,適用于治療既往經(jīng)過(guò)蛋白酶體抑制劑和免疫調(diào)節(jié)劑治療后無(wú)藥可選的多發(fā)性骨髓瘤���,本品獲批上市為此類(lèi)患者帶來(lái)了治療獲益����。
6.利妥昔單抗注射液�����,為國(guó)內(nèi)首個(gè)利妥昔單抗生物類(lèi)似藥注射液�����,同時(shí)也是國(guó)內(nèi)首個(gè)上市的生物類(lèi)似藥�,適用于治療非霍奇金淋巴瘤,本品獲批上市提高了此類(lèi)患者的臨床可及性���。
7.貝伐珠單抗注射液���,為國(guó)內(nèi)首個(gè)貝伐珠單抗注射液生物類(lèi)似藥,適用于治療轉(zhuǎn)移性結(jié)直腸癌�,晚期、轉(zhuǎn)移性或復(fù)發(fā)性非小細(xì)胞肺癌,本品獲批上市將提高該類(lèi)藥品的可及性�����。
抗感染藥物:
8.格卡瑞韋哌侖他韋片�,為全新的抗丙肝固定組合復(fù)方制劑,適用于治療基因1���、2��、3��、4、5或6型慢性丙型肝炎病毒(HCV)感染的無(wú)肝硬化或代償期肝硬化成人和12歲至18歲以下青少年患者�����,屬臨床急需境外新藥名單品種�����。本品針對(duì)全基因型在初治無(wú)肝硬化患者中的治療周期可縮短至8周�����,其獲批上市將進(jìn)一步滿(mǎn)足臨床需求���,為丙肝患者提供了更多治療選擇��。
9.索磷韋伏片��,為索磷布韋��、維帕他韋��、伏西瑞韋3種成分組成的固定復(fù)方制劑��,適用于治療慢性丙型肝炎病毒感染�����,屬臨床急需境外新藥名單品種���。本品可為全基因型既往直接抗病毒藥物(DAA)治療失敗的丙肝患者提供高效且耐受的補(bǔ)救治療方案�����,填補(bǔ)了臨床空白����。
10.拉米夫定替諾福韋片,為拉米夫定和替諾福韋二吡呋酯的固定劑量復(fù)方制劑�����,適用于治療人類(lèi)免疫缺陷病毒-1(HIV-1)感染����,屬?lài)?guó)內(nèi)首個(gè)仿制藥。拉米夫定片和替諾福韋二吡呋酯片的聯(lián)合治療方案為臨床抗HIV的一線治療方案���,本品獲批上市可提高患者的用藥依從性��。
11.注射用頭孢他啶阿維巴坦鈉���,為新型β-內(nèi)酰胺酶抑制劑,適用于治療復(fù)雜性腹腔內(nèi)感染���、醫(yī)院獲得性肺炎和呼吸機(jī)相關(guān)性肺炎、以及在治療方案選擇有限的成人患者中治療由革蘭陰性菌引起的感染���。本品獲批上市可解決日益突出的耐藥菌感染所帶來(lái)的巨大挑戰(zhàn)�,滿(mǎn)足了迫切的臨床治療要求��。
循環(huán)系統(tǒng)藥物:
12.波生坦分散片,為我國(guó)首個(gè)用于兒童肺動(dòng)脈高壓(PAH)的特異性治療藥物���,屬兒童用藥且臨床急需境外新藥名單品種�。PAH是一種進(jìn)展性的危及生命的疾病���,國(guó)內(nèi)尚無(wú)針對(duì)兒童PAH患者的特異性治療藥物�,本品為針對(duì)兒童開(kāi)發(fā)的新劑型���,其獲批上市解決了兒童PAH患者的用藥可及性�����。
風(fēng)濕性疾病及免疫藥物:
13.注射用貝利尤單抗�����,為一種重組的完全人源化IgG2λ單克隆抗體�����,適用于在常規(guī)治療基礎(chǔ)上仍具有高疾病活動(dòng)的活動(dòng)性�、自身抗體陽(yáng)性的系統(tǒng)性紅斑狼瘡(SLE)成年患者��,是全球近60年來(lái)首個(gè)上市用于治療SLE的新藥。目前SLE治療選擇不多�����,本品獲批上市滿(mǎn)足了SLE患者未被滿(mǎn)足的臨床需求�����。
14.阿達(dá)木單抗注射液�����,為國(guó)內(nèi)首個(gè)阿達(dá)木單抗生物類(lèi)似藥�����,適用于治療成年患者的類(lèi)風(fēng)濕關(guān)節(jié)炎�、強(qiáng)直性脊柱炎和銀屑病等自身免疫性疾病,本品獲批上市將提高該類(lèi)藥物的臨床可及性�����,有效降低患者經(jīng)濟(jì)負(fù)擔(dān)�����。
神經(jīng)系統(tǒng)藥物:
15.拉考沙胺片��,為新型抗癲癇藥物�,適用于16歲及以上癲癇患者部分性發(fā)作的聯(lián)合治療,屬?lài)?guó)內(nèi)首個(gè)仿制藥��,本品獲批上市提高了此類(lèi)患者的用藥可及性���,方便患者使用��。
16.咪達(dá)唑侖口頰粘膜溶液�����,為國(guó)內(nèi)首家治療兒童驚厥急性發(fā)作的口頰粘膜溶液�,屬兒童用藥�。小兒驚厥常為突然發(fā)作,靜脈注射�����、肌肉注射���、直腸給藥等給藥方式較為困難����,口頰粘膜給藥方式可彌補(bǔ)上述給藥途徑的不足,本品獲批上市為此類(lèi)患者提供了一項(xiàng)新的更便捷的給藥方式��。
鎮(zhèn)痛藥及麻醉科藥物:
17.水合氯醛灌腸劑���,適用于兒童檢查/操作前的鎮(zhèn)靜�����、催眠�����,以及監(jiān)護(hù)條件下的抗驚厥的中樞鎮(zhèn)靜藥物��,屬首批鼓勵(lì)研發(fā)申報(bào)兒童藥品清單品種�。本品是適合兒童應(yīng)用的劑型���,其獲批上市填補(bǔ)了國(guó)內(nèi)兒童診療鎮(zhèn)靜用水合氯醛制劑無(wú)上市品種的空白�,滿(mǎn)足我國(guó)兒科臨床迫切需求��。
皮膚及五官科藥物:
18.本維莫德乳膏����,為具有我國(guó)自主知識(shí)產(chǎn)權(quán)的全球首創(chuàng)治療銀屑病藥物,具有全新結(jié)構(gòu)和全新作用機(jī)制��,適用于局部治療成人輕至中度穩(wěn)定性尋常型銀屑病����。本品獲批上市為臨床提供了一種新型的安全有效治療藥物選擇。
19.司庫(kù)奇尤單抗注射液�����,為我國(guó)首個(gè)白介素類(lèi)治療中至重度銀屑病藥物�,屬臨床急需境外新藥名單品種。與TNFα類(lèi)藥物相比��,本品療效更好�����,其獲批上市為此類(lèi)患者提供了一種新作用機(jī)制的藥物選擇���。
罕見(jiàn)病藥物:
20.依洛硫酸酯酶α注射液�,為國(guó)內(nèi)首個(gè)且唯一用于治療罕見(jiàn)病IVA型黏多糖貯積癥(MPS IVA���,Morquio A綜合征)的酶替代治療藥物�,屬臨床急需境外新藥名單品種。黏多糖貯積癥是是嚴(yán)重危及生命且國(guó)內(nèi)尚無(wú)有效治療手段的疾病��,本品獲批上市填補(bǔ)了我國(guó)此類(lèi)患者的用藥空白����。
21.注射用阿加糖酶β,為治療罕見(jiàn)病法布雷病的長(zhǎng)期酶替代療法藥物����,屬臨床急需境外新藥名單品種。法布雷病是嚴(yán)重危及生命且國(guó)內(nèi)尚無(wú)有效治療手段的疾病����,已列入我國(guó)第一批罕見(jiàn)病目錄,本品獲批上市填補(bǔ)了國(guó)內(nèi)此類(lèi)患者的治療空白��。
22.諾西那生鈉注射液����,為國(guó)內(nèi)首個(gè)且唯一用于治療罕見(jiàn)病脊髓性肌萎縮癥的藥物,屬臨床急需境外新藥名單品種�。本品有效解決了我國(guó)脊髓性肌萎縮癥目前尚無(wú)有效治療手段的臨床用藥急需。
23.依達(dá)拉奉氯化鈉注射液,適用于治療罕見(jiàn)病肌萎縮側(cè)索硬化(ALS)����,屬臨床急需境外新藥名單品種。本品有效解決了目前我國(guó)ALS尚無(wú)有效治療手段的臨床用藥急需����。
預(yù)防用生物制品(疫苗):
24. 13價(jià)肺炎球菌多糖結(jié)合疫苗��,為具有自主知識(shí)產(chǎn)權(quán)的首個(gè)國(guó)產(chǎn)肺炎球菌結(jié)合疫苗����,適用于6周齡至5歲(6周歲生日前)嬰幼兒和兒童,預(yù)防1型�����、3型等13種血清型肺炎球菌引起的感染性疾病����。本品是全球第二個(gè)預(yù)防嬰幼兒和兒童肺炎的疫苗���,其上市提高了該類(lèi)疫苗的可及性����,可更好的滿(mǎn)足公眾需求���。
25.重組帶狀皰疹(CHO細(xì)胞)疫苗����,適用于50歲及以上成人預(yù)防帶狀皰疹�,屬臨床急需境外新藥名單品種。隨著年齡增長(zhǎng)���,帶狀皰疹患病風(fēng)險(xiǎn)升高�����,且其并發(fā)癥嚴(yán)重影響患者正常工作和生活���,目前國(guó)內(nèi)缺少對(duì)該疾病的有效預(yù)防和治療手段,本品獲批上市進(jìn)一步滿(mǎn)足了公眾特別是我國(guó)老齡患者的臨床用藥需求�����。
26.雙價(jià)人乳頭瘤病毒疫苗(大腸桿菌)����,為首個(gè)國(guó)產(chǎn)人乳頭瘤病毒(HPV)疫苗,適用于9~45歲女性預(yù)防由HPV16/18引起的相關(guān)疾病,9~14歲女性也可以選擇采用0��、6月分別接種1劑次的免疫程序��。本品可進(jìn)一步緩解國(guó)內(nèi)HPV疫苗的供需緊張�,有助于滿(mǎn)足我國(guó)女性對(duì)HPV疫苗的臨床需求。
中藥新藥:
27.芍麻止痙顆粒���,為白芍、天麻等11種藥味組成的新中藥復(fù)方制劑�����,屬兒童用藥��,可治療抽動(dòng)-穢語(yǔ)綜合征(Tourette綜合征)及慢性抽動(dòng)障礙中醫(yī)辨證屬肝亢風(fēng)動(dòng)�����、痰火內(nèi)擾者��。本品可明顯改善患兒的運(yùn)動(dòng)性抽動(dòng)�����、發(fā)聲性抽動(dòng),以及社會(huì)功能缺損���,精神神經(jīng)系統(tǒng)不良反應(yīng)發(fā)生率明顯低于已上市藥品之一的陽(yáng)性藥鹽酸硫必利片����,為患兒尤其是輕中度患兒提供了一種更為安全有效的治療選擇�����,滿(mǎn)足患者需求和解決臨床可及性����。
28.小兒荊杏止咳顆粒,為荊芥�、苦杏仁等12種藥味組成的新中藥復(fù)方制劑,屬兒童用藥���,具有“疏風(fēng)散寒��、宣肺清熱���、祛痰止咳”的功效,適用于治療小兒外感風(fēng)寒化熱的輕度支氣管炎���。本品在咳嗽�����、咳痰等主要癥狀改善和中醫(yī)證候��、疾病愈顯率等方面具有明顯療效���,不良反應(yīng)較少�����,為急性支氣管炎小兒患者提供了一種新的安全有效的治療選擇。